Alicia Callejón Callejón, Inmaculada Plasencia García*, Orlando Mesa Medina
Pediatra. Unidad de Neumología Pediátrica. *Servicio de Farmacia. Hospital Universitario Nuestra Señora de Candelaria
Introducción
El asma es un síndrome que incluye diversos fenotipos clínicos que comparten manifestaciones clínicas similares, pero de etiologías probablemente diferentes. En los últimos años se ha utilizado más esta definición, ya que clásicamente, se definía como una enfermedad inflamatoria crónica de las vías respiratorias que cursa con hiperrespuesta bronquial y una obstrucción variable al flujo aéreo, total o parcialmente reversible.
El diagnóstico de asma se debe considerar ante síntomas y signos clínicos de sospecha, como sibilancias, disnea o dificultad respiratoria, tos y opresión torácica. Las pruebas de función respiratoria pueden contribuir al diagnóstico, aunque su normalidad no lo excluye y no discriminan el nivel de gravedad. El objetivo de diagnosticar y tratar esta enfermedad es alcanzar y mantener el control de la patología y prevenir el riesgo futuro de exacerbaciones.
Uno de los pilares fundamentales del tratamiento es la educación integral del paciente asmático que junto con las nuevas terapias hace posible que se reduzca el riesgo de exacerbaciones y aumente la calidad de vida del paciente.
Asma grave infantil
Entre un 5-10 % de los niños con asma desarrolla asma grave, lo que constituye un problema sanitario importante teniendo en cuenta la elevada prevalencia de la enfermedad y el gran porcentaje de recursos que consume. Este grupo de niños asmáticos tiene más riesgo de exacerbaciones, atenciones en urgencias e ingresos hospitalarios, así como de presentar un asma más grave en la edad adulta.
Concepto de gravedad y control
El asma grave se caracteriza por la necesidad de precisar múltiples fármacos y a altas dosis para su tratamiento. La gravedad del asma no es una característica necesariamente constante, sino que puede variar a lo largo del tiempo, por lo que es necesario reevaluarla periódicamente.
El control del asma debe ser evaluado en cada consulta, y el tratamiento debe ajustarse para alcanzar y mantener el control. Se pueden utilizar cuestionarios validados de síntomas para objetivar el control. Debemos realizar historia clínica exhaustiva sobre síntomas, exacerbaciones, uso de medicación de rescate, comorbilidades, y solicitaremos pruebas de función pulmonar así como en casos individualizados, biomarcadores inflamatorios (eosinófilos sangre o esputo y FENO).
Asma grave no controlada en el niño
Asma grave no controlada en el niño es más frecuente a partir de la edad escolar con una prevalencia del 2-5 %. Tiene una elevada morbilidad, costes y riesgo futuro de enfermedad pulmonar obstructiva crónica. Su presentación clínica y respuesta al tratamiento varía del lactante al adolescente.
Según la edad del paciente diferenciamos:
- Lactantes que presentan exacerbaciones graves recurrentes, con o sin síntomas intercrisis, a pesar de un adecuado tratamiento y han tenido
- > 1 ingreso en una Unidad de Cuidados Intensivos
- > 2 ingresos hospitalarios que requieran tratamiento intravenoso o
- > 2 ciclos de glucocorticoides orales en el año previo
- Escolares y adolescentes con cuestionarios de calidad de vida compatibles (ACT <20) y limitación crónica al flujo aéreo tras uso de tratamiento
Hasta un 12-30 % de los pacientes con asma grave no controlado puede tener otro diagnóstico que simula los síntomas de asma.
Muchos niños con asma grave no controlada tienen una función pulmonar dentro de la normalidad, siendo necesario realizar una prueba de bronco provocación. Además, serán necesarios otros exámenes complementarios, orientados por la sospecha clínica o presentación atípica. Se debe investigar la existencia de comorbilidades y/o factores asociados, que son evitables e influyen en el control. Han de ser cuidadosamente evaluados: la falta de adhesión al tratamiento, una técnica de inhalación inadecuada, la exposición a alérgenos y al humo del tabaco. Todo ello no puede ayudar a tomar decisiones terapéuticas, como añadir anticuerpo monoclonal.
Fenotipos en asma grave del niño
Su investigación es necesaria para un adecuado tratamiento personalizado y en aquellos pacientes que su asma permanezca mal controlada y con exacerbaciones frecuentes, debe considerarse la adición de fármacos biológicos.
La inflamación tipo 2 en el asma abarca varios fenotipos de pacientes. La GINA y la GEMA recomiendan determinar este tipo de inflamación como un paso importante en el tratamiento del asma grave.
- Asma alérgic Es el fenotipo más común. Tiene una base atópica, orquestada por la activación de las células T colaboradoras tipo 2 (Th2), la producción de interleucina (IL) 4, IL-5 e IL-13 y el cambio de isotipo en los linfocitos B hacia la producción de IgE. Cursan con un patrón inflamatorio eosinofílico puro o mixto (eosinofilia y neutrofilia) en el esputo. La periostina (una proteína de la matriz celular inducida por la IL-13), que puede medirse en la sangre y las secreciones bronquiales, y la fracción de óxido nítrico exhalado son buenos biomarcadores de la variante T2 “elevada”. El diagnóstico requiere la demostración de la sensibilización a un alérgeno y el desencadenamiento de la sintomatología con la exposición a éste. Se asocian comorbilidades atópicas (rinitis alérgica, dermatitis atópica, alergia alimentaria) y un perfil inflamatorio T2 alto (IgE elevada, eosinofilia periférica y elevación de la FENO).
- Asma eosinofílica se caracteriza por la presencia de eosinófilos en las biopsias bronquiales y en el esputo, a pesar de un tratamiento con dosis altas de glucocortic Pueden cursar con rinosinusitis crónica y pólipos nasales. Aunque su prevalencia de atopia es menor, la IgE y la FENO pueden estar elevadas. En su patogenia están implicadas alteraciones en el metabolismo del ácido araquidónico. Una elevada producción de IL-5 puede explicar la inflamación eosinofílica en ausencia del clásico mecanismo T2 mediado por la alergia.
Los biomarcadores de inflamación de tipo 2 pueden verse suprimidos por el uso de OCS.
Nuevas terapias biológicas
Hoy en día disponemos en el mercado de tres tratamientos biológicos para el asma mal agrave infantil (tabla 1)
Omalizumab. Anticuerpo monoclonal anti-IgE que ha mostrado ser eficaz para el tratamiento de niños de 6 o más años con asma grave no controlada alérgica con sensibilización a alérgenos perennes con valores de IgE total entre 30-1.500 UI. La dosis varía en función del nivel de IgE y del peso corporal y la vía de administración es subcutánea cada 2 o 4 semanas. Con más de 15 años de experiencia en práctica clínica ha demostrado su eficacia en los ensayos aleatorizados controlados: reduce las exacerbaciones, la intensidad de los síntomas, el uso de medicación de rescate y mejora la calidad de vida.
Mepolizumab. Anticuerpo monoclonal anti-IL5, eficaz en asma grave eosinofílica (>300 eosinófilos/µl en sangre en el año previo o con > 150/µl en el momento del tratamiento). Actualmente existe indicación para su uso a partir de los 6 años de vida, disponiéndose de datos de seguridad y eficacia que apoyan su utilización en niños con asma grave eosinofílica, con un perfil similar al de los adolescentes y adultos. La dosis recomendada es de 40 mg entre los 6-11 años y 100 mg a partir de los 12 años, administrada por vía subcutánea, una vez cada cuatro semanas. Se ha comprobado reducción de exacerbaciones y reducción de la dosis de GCO en pacientes en tratamiento de mantenimiento con glucocorticoides sistémicos. En trabajos recientes se ha demostrado la efectividad de este fármaco en pacientes con respuesta parcial a omalizumab85. Indicado si existe rinosinusitis crónica con poliposis nasal y en granulomatosis con poliangeítis
Dupilumab. Anticuerpo monoclonal humano dirigido contra la cadena a del receptor de la IL-4 y que bloquea los efectos de la IL-4 e IL-13, está autorizado como tratamiento adicional en pacientes mayores de 12 años con asma grave no controlada con eosinófilos (>300 cel/μl ) y/o FENO elevados (>50 ppb), eosinofilia >150 cel/μl y FeNO >25 ppb + ≥ 2 exacerbaciones (o un ingreso) el año previo o corticodependiente oral, Además presente dermatitis atópica severa, o rinosinusitis crónica con poliposis nasal, o esofagitis eosinofílica
Bibliografía
- Iniciativa Global para el Asma (Global Initiative for Asthma, GINA). Estrategia global para el tratamiento y la prevención del asma, actualizada en https://ginasthma.org/gina-reports/
- Teague WG, Phillips BR, Fahy JV, Wenzel SE, Fitzpatrick AM, Moore WC, et al. Baseline features of the severe asthma research program (SARP III) cohort: differences with ag J Allergy Clin Immunol Pract 2018; 6:545-54
- Fleming L, Murray C, Bansal AT, Hashimoto S, Bisgaard H, Bush A, et al. The burden of severe asthma in childhood and adolescence: results from the paediatric U-BIOPRED c Eur Respir J. 2015; 46: 1322-33
- Holguin F, Cardet JC, Chung KF, Diver S, Ferreira DS, Fitzpatrick A et al. Management of severe asthma: a European Respiratory Society/American Thoracic Society Eur Respir J 2020; 55:1900588
- Chipps BE, Lanier B, Milgrom H, Deschildre A, Hedlin G, Szefler SJ et Omalizumab in children with uncontrolled allergic asthma: review of clinical trial and real-world experience. J Allergy Clin Immunol 2017; 139:1431-44
- Gupta A, Pouliquen I, Austin D, Price RG, Kempsford R, Steinfeld J et al. Subcutaneous mepolizumab in children aged 6 to 11 years with severe eosinophilic as Pediatr Pulmonol 2019; 54(12):1957- 67
- Farne HA, Wilson A, Powell C, Bax L, Milan SJ. AntiIL5 therapies for asthma (Review). Cochrane Database Syst Rev. 2017(9): CD010834
- Gupta A, Ikeda M, Geng B, Azmi J, Price RG, Bradford ES, Yancey SW, Steinfeld J. Long-term safety and pharmacodynamics of mepolizumab in children with severe asthma with an eosinophilic phenotype. J Allergy Clin Immunol 2019; 144(5):1336-42
- Corren J, Castro M, O’Riordan T, Hanania NA, Pavord ID, Quirce S et Dupilumab efficacy in patients with uncontrolled, moderate-to-severe allergic asthma. J Allergy Clin Immunol Pract 2020; 8:516-526
- Castro M, Corren J, Pavord ID, Maspero J, Wenzel S, Rabe KF et Dupilumab efficacy and safety in moderate-to-severe uncontrolled asthma. N Engl J Med 2018; 378:2486-2496
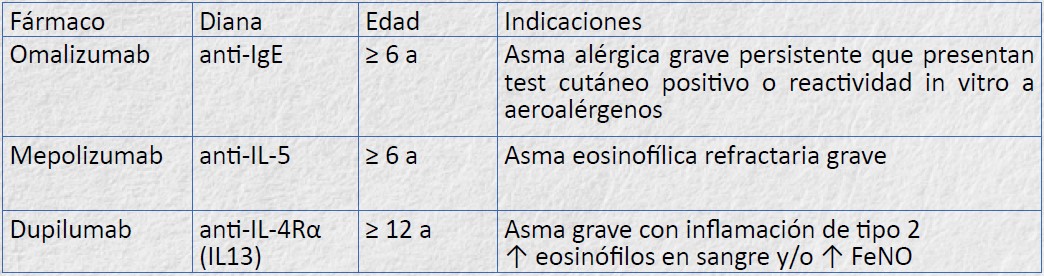
Tabla 1
