Laura Carrión1, Alba Lopezosa1, Silvia Escalada2, Lucía Garriga2
1 Médico residente de pediatría, 2 Médico pediatra del Servicio de Urgencias Pediátricas, Hospital Universitario de Canarias, Tenerife
Resumen
Introducción. Existe evidencia controvertida respecto a que la adición de bromuro de ipratropio a los beta 2 agonistas sea beneficiosa en el manejo de los broncoespasmos agudos moderados. Además, podría incrementar la aparición de efectos adversos.
Pacientes y métodos. Estudio unicéntrico, retrospectivo, caso-control de pacientes diagnosticados de broncoespasmo agudo moderado en urgencias de un hospital terciario durante dos periodos: “con uso de ipratropio” (1 de septiembre 31 de diciembre de 2015) y “sin uso de ipratropio” (1 de septiembre -31 de diciembre de 2019. Para alcanzar el tamaño muestral calculado, se incluyeron también las consultas entre el 1 de enero 28 de febrero de 2019 y entre el 1 de enero 29 de febrero de 2020). Se compararon las características demográficas, clínicas, el tratamiento recibido y la evolución.
Resultados. Se incluyeron 106 pacientes en el grupo con ipratropio y 100 pacientes en el grupo sin ipratropio. Las características demográficas y clínicas de ambos grupos fueron similares excepto los ingresos previos y el tratamiento de base. El tratamiento recibido en urgencias, excepto el ipratropio, fue similar. No hubo diferencias en los ingresos ni en las readmisiones en las siguientes 72 horas. No se encontró un aumento de los efectos adversos derivados de la utilización de ipratropio.
Conclusiones. En nuestro estudio, la adición de ipratropio al tratamiento con salbutamol y corticoterapia en pacientes con broncoespasmo agudo moderado no cambió la evolución de los pacientes. Tampoco se objetivó un aumento de los efectos adversos asociados a su uso.
Palabras clave: broncoespasmo agudo moderado, asma, bromuro de ipratropio, efectos adversos, seguridad
Effectiveness and safety of ipratropium bromide in moderate bronchospasms in the emergency department.
Abstract
Introduction. There is controversial evidence regarding the possible benefits that ipratropium bromide (IB) may add to beta 2 agonists in the management of moderate bronchospasms. Besides, the addition of IB to the treatment could increase adverse effects.
Patients and methods. A single-center, retropective and case-control study was coducted on a sample of patients diagnosed with moderate bronchospasm in the Emergency Department of a tertiary hospital during two periods: with use of ipratropium (September 1st to December
31st of 2015) and without use of ipratropium (September 1st to December 31st of 2019. To reach the calculated sample size, patients that were attended from January 1st to February 28th of 2019 and from January 1st to February 29th of 2020 were also included). We compared demographic and clinical characteristics, treatment received and evolution between both periods.
Results. 106 patients were included in the “with use of ipratropium” group and 100 patients were included in the “without use of ipratropium” group. Demographic and clinical characteristics of both groups were similar. There were not differences in hospital admission rate or re-assessments in the Emergency Department between both groups. We did not found an increase in the adverse effects derived from the use of IB either.
Conclusions. In our study, the addition of IB to salbutamol and corticosteroids in the treatment of moderate bronchospasms did not change the evolution of the patients. We did not objectified an increase in the adverse events rate in patients treated with IB either.
Key words: moderate bronchospasms, asthma, ipratropium bromide, adverse effects, safety
Introducción
El asma es la enfermedad crónica más frecuente en los niños1. En España la prevalencia del asma en pediatría se sitúa en torno al 10 %, con variaciones entre comunidades2. Las exacerbaciones asmáticas suponen la urgencia médica más frecuente en pediatría y constituyen alrededor del 5% de los motivos de consulta, llegando a alcanzar en torno a un 15 % en los meses epidémicos3. La tasa de ingreso en planta o en observación de los servicios de urgencias (SU) de los pacientes con exacerbaciones se sitúa alrededor del 15 % siendo menor, pero no desdeñable, la tasa de ingresos en unidades de cuidados intensivos pediátricos (UCIP)3. Además se estima que las exacerbaciones son responsables de más del 80 % de los costes directos asociados al asma4,5, representando un coste económico considerable para los sistemas de salud1.
El tratamiento de las crisis asmáticas se basa en el uso de fármacos broncodilatadores junto con corticoides en las exacerbaciones moderadas y graves. Los beta 2 agonistas de acción corta constituyen el pilar del tratamiento broncodilatador por su potente y rápido efecto sobre la musculatura lisa bronquial. El bromuro de ipratropio (BI) es un agente anticolinérgico que proporciona broncodilatación mediante relajación del músculo liso bronquial. Su inicio de acción es más lento y más débil en comparación con los beta 2 agonistas. Ensayos aleatorizados, revisiones sistemáticas y metaanálisis han demostrado que el tratamiento combinado de bromuro de ipratropio con beta2 agonista en las exacerbaciones severas (Pulmonary Score “PS”: 7-9) reduce la tasa de ingresos hospitalarios en comparación con sólo beta 2 agonista6,7. El manejo de las exacerbaciones leves (PS 0-3) es satisfactorio, en la mayoría de las ocasiones, con el uso exclusivo de beta2 agonistas2. Sin embargo, la evidencia existente respecto a que la asociación de fármacos beta 2 agonistas con bromuro de ipratropio suponga algún beneficio en el manejo de las exacerbaciones moderadas (PS 4-6) en comparación con sólo beta 2 agonistas es controvertida. De hecho, un estudio reciente objetiva un aumento no significativo de la tasa de ingresos con la asociación de ambos fármacos en comparación con sólo beta2 agonistas en los broncoespasmos moderados8. Por otro lado, la adición de bromuro de ipratropio al tratamiento broncodilatador podría incrementar la aparición de efectos adversos8.
El objetivo de este estudio es determinar la efectividad y seguridad de la administración conjunta de bromuro de ipratropio y salbutamol en el tratamiento de las exacerbaciones moderadas en nuestro centro.
Pacientes y métodos
Se diseñó un estudio unicéntrico en un hospital terciario, retrospectivo analítico observacional tipo caso-control de los pacientes diagnosticados de bronsoespasmo agudo (BA) moderado en el SU durante dos periodos epidémicos: “con uso de BI” en BA moderados (septiembre octubre, noviembre y diciembre de 2015) y “sin uso de BI” en BA moderados (septiembre, octubre, noviembre y diciembre de 2019). Para alcanzar el tamaño muestral calculado en el grupo “sin BI”, se tuvo que ampliar el periodo de estudio desde el 1 de enero al 28 de febrero de 2019 y desde el 1 de enero al 29 de febrero de 2020 (figura 1). Se revisaron las historias clínicas de los pacientes. Según la literatura disponible, el porcentaje de ingresos en pacientes con BA moderado se sitúa en torno al 40-44 %8. Para calcular el tamaño muestral, nos basamos en la revisión de Benito Fernández et al. Quien encuentra una diferencia del 18 % en la proporción de ingresos entre pacientes “con y sin uso de BI” en su asistencia en el SU9. En base a ella, nos marcamos como objetivo detectar un cambio en el porcentaje de ingresos del 20 %, asumiendo un riesgo alfa del 5 % y un riesgo beta del 10 %. El tamaño muestral requerido para conseguir el objetivo descrito fue de 82 pacientes por grupo de tratamiento, decidiendo incluir al menos 100 pacientes por cada grupo de tratamiento.
Para realizar el estudio estadístico, las variables cuantitativas se describieron con medidas de centralización y de dispersión: media con desviación estándar (desv.est) y mediana con rango intercuartílico (RIQ). Las variables cualitativas se describieron mediante frecuencias absolutas (N) y relativas (%). Para estudiar las diferencias entre los 2 grupos de estudio “con y sin uso de BI”, las variables cuantitativas se compararon mediante la “t” de Student si seguían una distribución normal y mediante la prueba U de Mann-Whitney si no existía distribución normal. Las variables cualitativas se compararon mediante el test de Chi cuadrado o test exacto de Fisher cuando éste estuvo indicado. Se consideró significación estadística una p<0,05. Los datos se analizaron con el programa SPSS 20.
Definiciones
Broncoespasmo agudo moderado: episodio brusco de dificultad respiratoria y sibilancias, con una puntuación en la puntuación de gravedad Pulmonary Score (PS) equivalente a moderada (4-6). En este estudio se prefiere hablar de broncoespasmo agudo en lugar de crisis asmática porque no todos los pacientes que acuden al SU con clínica de broncoespasmo han sido diagnosticados de asma.
Criterios de inclusión
Niños entre 2 y 14 años con diagnóstico de BA moderado al alta del SU
Criterios de exclusión
Pacientes < 2 años: Con el objetivo de evitar el posible solapamiento con bronquiolitis aguda.
- Pacientes ≥ 15 años: en el SU del centro hospitalario donde se realizó el estudio, se atiende a pacientes hasta los 15 años.
- Pacientes con antecedente personal de enfermedad respiratoria crónica (neumopatías intersticiales, fibrosis pulmonares, fibrosis quística, bronquiolitis obliterante, discinesia ciliar primaria), enfermedad neuromuscular, parálisis cerebral o cardiopatía c
- Pacientes que hayan recibido bromuro de ipratropio en las seis horas previas a su visita a urgencias
- Broncoespasmos leves (PS 0-3) o graves (PS 7-9)
Recogida de datos
Se recogieron los siguientes datos:
- Demográficos: Fecha de atención, edad, sexo, comorbilidad, ingresos previos por broncoespasmo, tratamiento de mantenimiento de asma.
- Clínicos: Salbutamol en las seis horas previas a su visita a urgencias, Corticoterapia en las 24 horas previas a su visita a urgencias, presencia de fiebre, saturación de oxígeno a su llegada al SU, frecuencia respiratoria y cardiaca a su llegada al SU, temperatura a su llegada al SU, puntuación de Pulmonary Score a su llegada al SU.
- Tratamiento: salbutamol nebulizado o inhalado en el SU, BI nebulizado o inhalado en el SU, corticoterapia en el SU, sulfato de magnesio en el SU, oxígeno en el SU
- Efectos adversos: Presencia/ausencia y tipo.
- Evolución: Destino (ingreso hospitalario, en UCIP o alta a domicilio), readmisión en las siguientes 72 horas con ingreso (en UCIP o planta de hospitalización), readmisión en las siguientes 72 horas sin ingr
Aspectos éticos
Este estudio se ajustó a las directrices del Convenio de Oviedo y de la Convención de Helsinki y fue aprobado por el comité ético de investigación clínica del hospital.
Resultados
Durante los meses de septiembre, octubre, noviembre y diciembre de 2015 (grupo caso: “con BI”) y los mismos meses de 2019, además de los meses de enero y febrero de 2019 y de 2020 (grupo control: “sin BI”) se diagnosticaron 224 y 320 BA moderados respectivamente. Tras aplicar los criterios de exclusión se incluyeron finalmente 106 pacientes en el grupo caso y 100 pacientes en el grupo control (figura 1).
Características demográficas y clínicas
Las características de ambos grupos fueron similares a excepción de los ingresos previos y el tratamiento de base, objetivándose más ingresos previos y mayor porcentaje de pacientes con tratamiento de base en el grupo SIN BI (tabla I). La clínica de presentación de los pacientes también fue similar a excepción del tratamiento corticoideo recibido 24 horas antes de su atención y la puntuación en el PS, siendo más frecuente el tratamiento corticoideo y mayor la puntuación en el PS grupo SIN BI. (tabla II).
Tratamiento
Todos los pacientes del grupo caso y ninguno de los pacientes del grupo control recibieron BI. La vía de administración en el total de pacientes del grupo “con BI” fue la nebulizada. La mediana de dosis fue de 250 mcg (RIQ: 250 mcg 250 mcg).
Todos los pacientes de ambos grupos recibieron salbutamol. En el grupo caso la vía de administración fue nebulizada en el 100% de los pacientes con una mediana de dosis de 2,7 mg (RIQ: 2,2 mg 4 mg) (Tabla III). En el grupo control la vía de administración más empleada siguió siendo la nebulizada en el 72 % vs. inhalada en el 28 %. La mediana de dosis empleada en vía nebulizada fue de 2,5 mg (RIQ 2 mg -3,75 mg). En la vía inhalada la media fue de 5 ± 1,4 inhalaciones. No hubo diferencias significativas entre ambos grupos en cuanto a la dosis de salbutamol nebulizada empleada. La variación en la vía de administración del tratamiento entre los dos grupos estuvo en relación con la implantación de un protocolo de manejo de los BA en el SU que se llevó a cabo en el año 2016 y que tenía como objetivo promover la utilización del tratamiento inhalado en BA leves y moderados.
Ambos grupos recibieron corticoterapia de forma similar, con una dosis entre 1-2 mg/Kg de prednisolona y prednisona. Dos pacientes del grupo control recibieron dexametasona y dos pacientes del grupo caso recibieron otro tipo de corticoterapia (uno hidrocortisona y uno metilprednisolona).
En cuanto al empleo de sulfato de magnesio en urgencias, se empleó en ocho pacientes del grupo “con BI” y en ningún paciente del grupo “sin BI”.
No se encontraron diferencias en cuanto a la necesidad de oxigenoterapia en urgencias entre ambos grupos de tratamiento.
Efectos adversos
No se encontraron efectos adversos atribuibles al BI, encontrándose tres pacientes en cada grupo aquejados de náuseas/ vómitos (2,8 % en grupo caso vs. 3 % en grupo control, con p= 1)
Evolución
No hubo diferencias significativas en la tasa de ingreso entre ambos grupos. Tampoco en la tasa de ingreso en UCIP ni en la readmisión en urgencias en las 72 horas siguientes (tabla IV). Respecto a la tasa de reconsultas con ingreso, ningún paciente del grupo “con BI” y cuatro pacientes del grupo SIN BI precisaron ingreso en la segunda consulta con una diferencia que está cerca de alcanzar significación estadística. Ninguno de los cuatro pacientes que ingresaron lo hizo en UCIP.
Discusión
En vista de los resultados expuestos, el tratamiento de los BA moderados con BI añadido a salbutamol y corticoterapia no reduce ni aumenta la proporción de ingresos en planta, en UCIP ni las readmisiones en las siguientes 72 horas en urgencias respecto al tratamiento con salbutamol y corticoterapia. Por otro lado, no se encontró un aumento de los efectos adversos derivados de la utilización de BI en el SU. Contrariamente a nuestros resultados, ensayos previos han encontrado un efecto beneficioso sobre la función pulmonar y otras variables en la adición de BI de forma precoz en combinación con salbutamol. Sin embargo, dichos ensayos sólo obtuvieron una tasa de ingresos global significativamente menor en el grupo “con BI” respecto al grupo “sin BI” cuando incluyeron una mayor proporción de pacientes graves10,11, mientras que la reducción de ingresos no fue significativa cuando los pacientes con BA moderados representaron la mayor parte de la muestra de los estudios9,12.
Los ensayos que incluyeron exclusivamente pacientes con BA moderados12,13 obtuvieron resultados contradictorios. Mientras que Sharma et al. objetivó una reducción significativa en la tasa de ingresos a favor del grupo “con BI”, Wyatt et al, detectó una mayor tasa de ingresos en el dicho grupo, aunque de forma no significativa8. Cabe destacar que el estudio de Sharma et al. tiene importantes limitaciones, como el pequeño tamaño muestral y la poca claridad en la graduación de la severidad del BA13. Por el contrario, el estudio de Wyatt et al. cuenta con importantes fortalezas como un amplio tamaño muestral y su validez interna y externa. Nuestros resultados coinciden los de Wyatt et al. habiendo observado una mayor tasa de ingresos en el grupo “con BI” de forma no significativa. En la última revisión sistemática, Griffiths et al. concluyeron que los BA tienen menor riesgo de ingresar si son tratadas con tratamiento combinado (beta 2 agonista y anticolinérgico) frente a sólo beta 2 agonistas, sugiriendo que la adición de BI puede tener un mayor beneficio a mayor gravedad del BA6. Sin embargo, no alcanzaron significación estadística por subgrupos de gravedad. No obstante, esta revisión no incluye el ensayo clínico de Wyatt et al. (que posee el mayor número de pacientes con BA moderados hasta la fecha), ya que dicho ensayo es posterior a la publicación de la revisión.
La Guía de práctica clínica española para el manejo del asma recomienda añadir BI en dosis frecuentes durante las dos primeras horas de tratamiento en los casos de BA moderado que no responden al tratamiento inicial con salbutamol2.
Por tanto, siguiendo en la línea de las últimas publicaciones y pese a que aún no se ha identificado qué subgrupo de pacientes con BA moderado podrían beneficiarse de la adición de BI desde el inicio del tratamiento, parece razonable pensar que debería reservarse para aquellos pacientes con mayor puntuación del PS o presencia de otros factores de riesgo de mala evolución como asma de mayor severidad o de peor control.
Sin embargo, las diferencias significativas halladas en las variables “tasa de ingresos previos” y “tratamiento de base”, ambas más frecuentes en el grupo SIN BI, podrían sugerir que los pacientes de ambos grupos no parten de una situación basal similar, sino que el grupo SIN BI está formado por pacientes con asma de mayor severidad o de peor control y, por tanto, con mayor probabilidad de ingreso. Pese a no haber utilizado BI, este grupo no ingresó en mayor proporción, lo que tampoco justificaría el empleo sistemático de BI en pacientes con historia de ingresos previos por BA o tratamiento de base.
En la misma línea, la diferencia hallada en la variable “puntuación del PS”, siendo mayor la puntuación del PS en el grupo SIN BI, podría indicar que los episodios fueron más severos en dicho grupo. Pese a ello, el tratamiento con salbutamol y corticoterapia parece ser suficiente al no haber ocasionado un aumento de los ingresos en este grupo. Por otro lado, la diferencia en la variable “tratamiento corticoideo previo”, habiendo sido más frecuentemente administrado previo a su valoración en el SU en el grupo SIN BI, podría haber supuesto cierto beneficio en este grupo, ya que en inicio de acción del corticoide habría empezado antes y podría haber contribuido a una mejor evolución.
Respecto a la evolución de los pacientes en urgencias, obtuvimos que, en el grupo “con BI”, se empleó sulfato de magnesio en
8 pacientes y no se empleó en ningún paciente del grupo “sin BI”. Dado el reducido número de pacientes que precisaron dicho broncodilatador intravenoso, no podemos comparar ambos grupos en este aspecto. En cuanto a la aparición de efectos adversos en relación con el uso de BI, la mayor parte de la evidencia actual es congruente con nuestros resultados9-18. Sin embargo, Wyatt et al. encontraron una tasa de efectos adversos significativamente mayor en el grupo “con BI” respecto al grupo “sin BI”, particularmente de temblor8. Griffiths et al. concluyeron en su revisión que los pacientes con BA tratados con BI presentaron menos temblor y náusea que los pacientes que no lo recibieron6, pero no incluyeron el ensayo de Wyatt et al., como previamente se ha comentado.
Respecto a la dosis de salbutamol nebulizado, si bien fue variable, en muchos casos se administró una dosis equivalente a 0,15 mg/Kg. Como resultado, los pacientes con un peso inferior a 16 Kg recibieron una dosis inferior a la que hoy en día se considera mínima terapéutica (2,5 mg), lo que podría haber provocado que dichos pacientes evolucionaran peor independientemente del uso de BI. Sin embargo, esta pauta estuvo presente en ambos grupos, por lo que, si existiera una mala evolución derivada del empleo de dosis bajas de salbutamol, sería esperable en ambos grupos por igual. De forma similar, pero con mayor importancia para este estudio, se obtuvo que la mediana de dosis de BI en el grupo “con BI” fue de 250 mcg, que hoy en día se considera mínima terapéutica. Sin embargo, en algunos pacientes se emplearon dosis inferiores (mínima dosis de 125 mcg). El empleo de dosis bajas de ipratropio podría haber impedido una mejor evolución de los pacientes del grupo “con BI”.
Nuestro estudio tiene varias limitaciones. Entre las inherentes a los estudios retrospectivos y caso-control, destaca la imposibilidad de recoger algunos datos importantes como la estancia media en el SU y las constantes al alta. Además, puede no haberse incluido en la historia clínica otros datos importantes para el estudio.
Otra limitación que puede ser importante es la diferencia que existe entre ambos grupos respecto a la situación basal de los pacientes. Como ya se ha comentado previamente el grupo “sin BI” tiene mayor tasa de ingresos previos y más tratamiento de base. Puede ser que al tratarse de grupos heterogéneos respecto a su situación basal las conclusiones de efectividad no sean totalmente válidas. Por ello, las conclusiones que se extraen de nuestro estudio deberían ser comprobadas con estudios de mayor calidad.
Por otro lado, el tamaño muestral es pequeño para tratarse de un estudio retrospectivo. en nuestro estudio, se marcó como objetivo detectar un cambio en el porcentaje de ingresos del 20 %. Sin embargo, dada la alta prevalencia de los BA moderados en pediatría, porcentajes de ingreso menores al 20 % tienen importante repercusión en lo que a gasto sanitario y repercusión familiar se refiere. Si se hubiera marcado como objetivo un porcentaje de ingresos menor al 20 %, el número de pacientes debería haber sido mayor para obtener resultados significativos.
Como limitación menor, cabe destacar que pese a la sectorización de la asistencia sanitaria en el área de salud donde se ha llevado a cabo el estudio, pueden haberse producido pérdidas en el seguimiento de los pacientes.
Bibliografía
- Global Initiative for As Global Strategy for Asthma Management and Prevention. National Heart, Lung and Blood Institute. National Institutes of Health, Bethesda. Online Appendix 2020[en línea] [consultado el 28/07/2021]. Disponible en: www.ginasthma.org
- Guía Española para el Manejo del Asma 2020 (GEMA 5.0) [en línea] [consultado el28/07/2021]. Disponible en: www.gcom
- Paniagua Calzón N, Benito Fernández J. Diagnóstico y tratamiento de la crisis asmática en Urg Protoc diagn ter pediatr 2020; 1:49-61
- Fanta CH. As N Engl J Med 2009; 360:1002-1014
- Akinbami LJ, Schoendorf K Trends in childhood asthma: Prevalence, health care utilization, and mortality. Pediatrics 2002;110:315-322
- Griffiths B, Ducharme FM. Combined inhaled anticholinergics and short-acting beta2agonists for initial treatment of acute asthma in childr Cochrane Database Syst Rev 2013;CD000060.
- Rodrigo GJ, Castro-Rodriguez JA. Anticholinergics in the treatment of children and adults with acute asthma: a systematic review with meta-analy Thorax 2005; 60:740
- Wyatt EL, Borland ML, Doyle SK, Geelhoed GC. Metered-dose inhaler ipratropium bromide in moderate acute asthma in children: a single-blinded randomised controlled J Paediatr Child Health 2015; 51:192-198
- Benito Fernández J, Mintegui Raso S, Sánchez Echaniz J, Vázquez Ronco MA, Pijoan Zubizarreta Efficacy of early administration of nebulized ipratropium bromide in children with asthmatic crisis. An Esp Pediatr 2000; 53:217-222
- Iramain R, Lopez-Herce J, Coronel J, Spitters C, Guggiari J, Bogado Inhaled salbutamol plus ipratropium in moderate and severe asthma crises in children. J Asthma 2011; 48:298-303.
- Qureshi F, Pestian J, Davis P, Zaritsky A. Effect of nebulized ipratropium on the hospitalization rates of children with as N Engl J Med 1998; 339:1030-1035
- Watanasomsiri A, Phipatanakul W. Comparison of nebulized ipratropium bromide with salbutamol vs salbutamol alone in acute asthma exacerbation in childr An Allergy Asthma Immunol 2006; 96:701-706
- Sharma A, Madaan A. Nebulized salbutamol vs salbutamol and ipratropium combination in as Indian J Pediatr 2004; 71:121-124
- Ducharme FM, Davis Randomized controlled trial of ipratropium bromide and frequent low doses of salbutamol in the management of mild and moderate acute pediatric asthma. J Pediatr 1998; 133:479-485
- Kumaratne M, Gunawardane Addition of ipratropium to nebulized albuterol in children with acute asthma presenting to a pediatric office. Clin Pediatr 2003; 42:127-132
- Qureshi F, Zaritsky A, Lakkis H. Efficacy of nebulized ipratropium in severely asthmatic childr Ann Emerg Med 1997; 29:205-211
- Reisman J, Galdes-Sebalt M, Kazim F, Canny G, Levison Frequent administration by inhalation of salbutamol and ipratropium bromide in the initial management of severe acute asthma in children. J Allergy Clin Immunol 1988; 81:16-20
- Schuh S, Johnson DW, Callahan S, Canny G, Levison Efficacy of frequent nebulized ipratropium bromide added to frequent highdose albuterol therapy in severe childhood asthma. J Pediatr 1995; 126:639-645
Figura 1. Selección de pacientes

Tabla I. Características demográficas

Tabla II. Características clínicas

Tabla III. Tratamiento en el Servicio de Urgencias
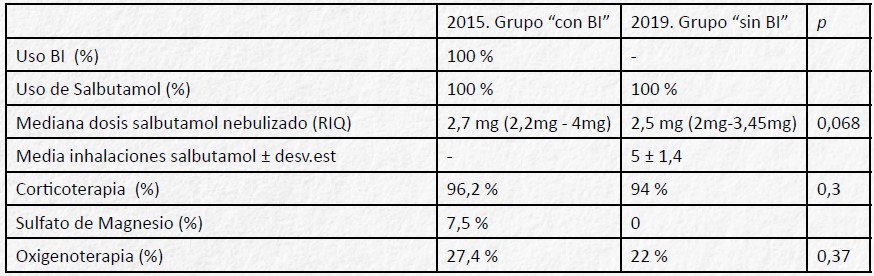
Tabla IV. Evolución

