María Hernández Apolinario1, Elena Caballero Estupiñán2, Héctor Ageno Alemán2, Zeltia García Suárez2
1FEA de Urgencias de Pediatría
2MIR de Pediatría
Servicio de Urgencias de Pediatría del Complejo Hospitalario Universitario Insular-Materno Infantil de Las Palmas de Gran Canaria
Resumen
Las fracturas patológicas se definen como aquellas causadas en un hueso debilitado, de manera local o sistémica, por un traumatismo de una energía que no causaría ningún daño en un hueso sano. Cuando se nos presenta un caso de fractura patológica en urgencias, hay que tener en mente un amplio abanico de diagnósticos diferenciales que abarcan desde alteraciones del metabolismo fosfocálcico, a tumores óseos tanto benignos como malignos, leucemia y otras entidades más infrecuentes como la displasia fibrosa ósea u osteomielitis. En el siguiente artículo presentamos un caso clínico de una paciente de 6 años que acude a nuestro servicio por dolor lumbar tras una caída de bajo impacto y en el que se evidencian fracturas patológicas vertebrales en las pruebas de imagen
Palabras claves: dolor lumbar, fracturas patológicas, leucemia, osteoporosis, raquitismo, displasia fibrosa, metabolismo fosfocálcico.
Abstract
Pathological fractures are defined as those fractures caused in a weakened bone that might be due to a local or a general process
by the trauma of such energy that would not cause any damage in a healthy bone. When we receive a case of pathological fracture in the emergency department, we must keep in mind a wide range of differential diagnoses that comprise alterations in phosphocalcic metabolism, benign and malignant bone tumours, leukaemia and other infrequent diseases such as fibrous bone dysplasia or osteomyelitis. In the following article, we present a clinical case of a 6-year-old patient who comes to our service for low back pain after a low impact fall, in which we can see pathological vertebral fractures in the radiographs.
Keywords: low back pain, pathological fractures, leukaemia, osteoporosis, rickets, fibrous bone dysplasia, phosphocalcic metabolism
Introducción
Las fracturas patológicas pediátricas presentan una baja frecuencia y constituyen un signo de alarma debido a que suelen esconder una patología subyacente. La presentación clínica más frecuente suele ser dolor musculoesquelético. En el caso de las fracturas vertebrales, la manifestación típica es en forma de dolor lumbar. Dicha patología, requiere una adecuada anamnesis y exploración física debido a que, a pesar de que en el 90% de los casos son dolores inespecíficos que no necesitan pruebas complementarias, es importante no subestimar el 10% restante, puesto que tienen un origen orgánico potencialmente grave1,2.
Entre los signos de alarma que requerirían una prueba de imagen en un dolor lumbar, podemos encontrar: fiebre, inmunosupresión, pérdida de peso, antecedentes de enfermedad neoplásica, osteoporosis, o traumatismo, tratamiento con glucocorticoides, anestesia en silla de montar, retención aguda de orina o incontinencia, dolor nocturno que no cede con antiinflamatorios entre otros. En el caso de objetivar fracturas patológicas, debemos tener en mente patología infecciosa (osteomielitis, discitis), patología tumoral (tumores óseos malignos y benignos, tumores sólidos, leucemia, linfoma) y alteraciones del metabolismo fosfocálcico (raquitismo, hiperparatirodismo, osteogénesis imperfecta, displasia fibrosa, osteoporosis idiopática, etc.)2-6.
Caso clínico
Niña de seis años sin antecedentes personales de interés, que acude al servicio de urgencias del hospital derivada de un centro de salud porque, según refiere, unas 24 horas previas a la consulta, sufre una caída desde su propia altura con impacto directo en región glútea. Tras la caída, presenta dolor lumbar que aumenta con el movimiento que no cede tras la administración de ibuprofeno y tiene dificultad para la movilización de los miembros inferiores de predominio izquierdo. Debido a la persistencia del dolor y a la dificultad para la movilización, refiere una nueva caída desde su propia altura con incapacidad posterior para mantener la posición de bipedestación.
Añade que, desde hace dos meses, padece episodios semanales esporádicos de dolor lumbar que no requieren analgesia y que se alivian con reposo.
No ha presentado cuadros febriles de repetición. No existe pérdida de peso ni astenia. No presenta síntomas miccionales ni incontinencia de esfínteres. No refiere ninguna otra sintomatología.
En la exploración física destaca una posición en decúbito supino con incapacidad para incorporarse. Presenta apofisalgia a nivel de T12-L1 con dolor a la flexo-extensión de ambas caderas sin presentar equimosis, deformidad ni otras alteraciones. Se solicitaron pruebas radiológicas. La radiografía de cadera fue normal. Las radiografías de columna lumbosacra AP y lateral (figura 1) y las radiografías dorsal AP y lateral (figura 2) mostraron fracturas de hundimiento en L2, D4 y D9.
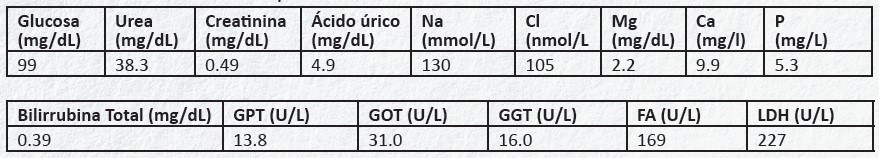
Tras objetivarse dichas lesiones, características de fracturas patológicas, se decide completar el estudio solicitando una analítica sanguínea con hemograma (Tabla 1), bioquímica (Tabla 2) y estudio de la coagulación.
En el frotis se observó una leucopenia con linfocitosis relativa y presencia de unos elementos de pequeño tamaño con escaso citoplasma. Trombopenia sin agregados plaquetares.
Figura 1. a) Hundimiento del platillo superior del cuerpo vertebral L2 con una pérdida de altura de un 25%. b) Hallazgo en relación con una fractura por compresión (flecha)
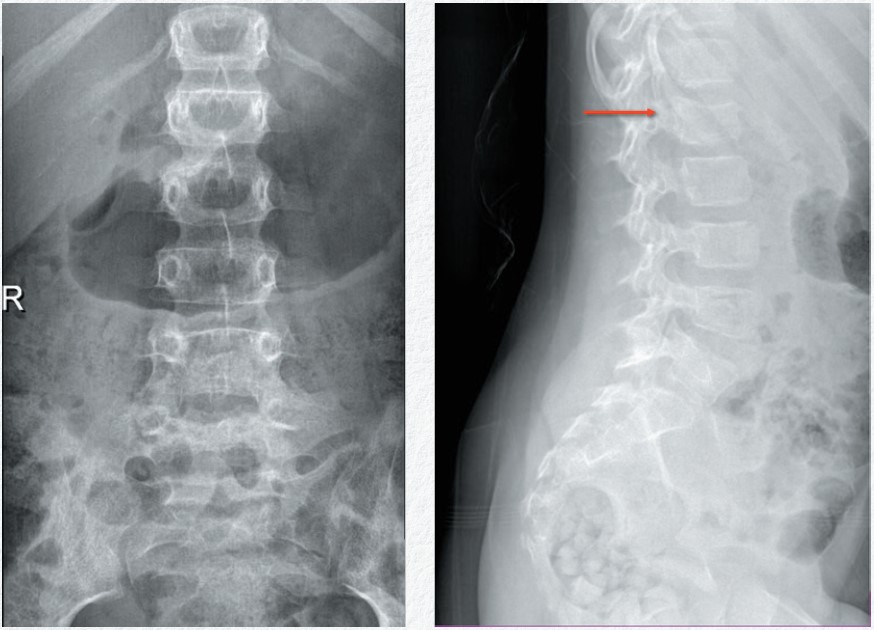
Tabla 1. Resultados del hemograma

Figura 2. a) Hundimiento de los platillos superiores con pérdida de altura menor de 25% de los cuerpos vertebrales D4 y D9. b) Hallazgo en relación con fractura por compresión (flechas)
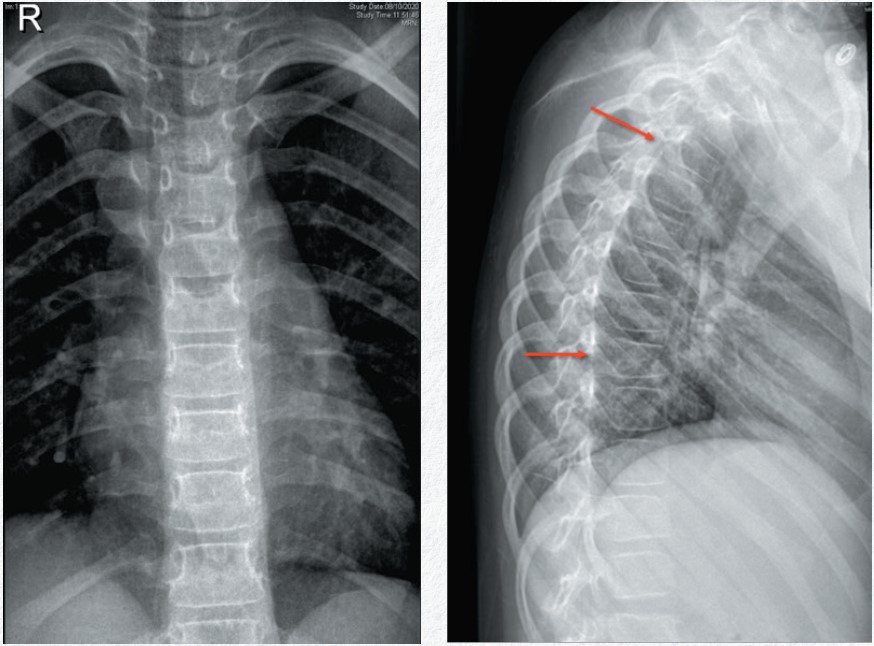
Tabla 2. Resultados de la bioquímica
Estudio de la coagulación normal
Ante los resultados del frotis con sospecha de leucemia aguda linfoblástica, es valorada por el Servicio de Hematología, que decide ampliar el estudio con un aspirado de médula ósea.
En el aspirado de médula ósea se observó una infiltración por un 87% de blastos de talla media con escaso citoplasma basófilo y núcleo con cromatina relativamente densa en la que no se evidencia nucléolo claro.
En la biopsia de médula ósea se objetivaron cilindros de médula ósea hipercelular (> 95 %), densamente infiltrada por una población atípica de características blásticas, sobre un fondo con representación y maduración de las tres series hematopoyéticas. Fibrosis reticulínica grado 0-1. No se observaro aumento de los depósitos de hierro.
Inmunohistoquímica de la población atípica: presenta positividad de tinción para CD10, CD79 y, débil y focalmente, para CD19 y CD20; siendo negativa para CD3 y CD7.
Con las técnicas para CD34 y TDT se contabilizan aproximadamente un 70% de blastos. Los hallazgos son compatibles con tejido medular óseo densamente infiltrado por una población linfoide, sugestivo de leucemia aguda linfoblástica B. Se inició tratamiento quimioterápico con un ciclo de inducción consistente en asparraginasa, vincristina, danorrubicina y corticoides.
Discusión
Ante todo dolor lumbar, lo primero que tenemos que hacer es descartar signos de alarma mediante una buena anamnesis y exploración física, dado que el 90% de los dolores lumbares que acuden a consulta son dolores inespecíficos que no requieren pruebas de imagen para su diagnóstico3,4. En nuestro caso, la paciente presentaba signos de alarma tales como antecedentes de traumatismo y dolor que no cede con analgesia, por lo que se decidió realizar pruebas de imagen en las que se objetivaron fracturas patológicas.
Ante cualquier fractura patológica, debemos plantearnos un amplio diagnóstico diferencial, destacando las siguientes patologías: alteración del metabolismo fosfocálcico, tumores óseos, displasia fibrosa ósea (síndrome de McCune-Albright), osteomielitis aguda o trastorno de la conducta alimentaria. Y, de forma complementaria, debemos solicitar un hemograma, una bioquímica con marcadores de fosfato cálcico y una coagulación.
Tras los resultados de las pruebas complementarias, el diagnóstico principal de sospecha es una leucemia, una neoplasia maligna a partir de la transformación maligna de una célula progenitora linfoide o mieloide inmadura que tiene la capacidad de expandirse y formar un clon de células progenitoras idénticas bloqueadas en un punto de diferenciación. Es la forma más frecuente de presentación del cáncer infantil.
La clínica más común de una leucemia aguda linfoblástica consiste en alteraciones hematológicas y fiebre. También puede presentar dolor óseo, pero es raro un debut de leucemia en forma de fractura patológica7-9.
Otros síntomas que pueden aparecer son: hepatoesplenomegalia, anorexia, infiltración testicular y masas mediastínicas7.
Ante la sospecha de leucemia, se deberá extraer un hemograma para confirmar el diagnóstico10. Dicho hemograma objetivará leucocitosis (a expensas de linfoblastos), leucopenia o leucocitos totales normales, anemia y trombopenia. En la extensión de sangre periférica se observarán linfoblastos, y en la biopsia de médula ósea se realizará un análisis morfológico, molecular y citogenético que presentará, al menos, un 20% de blastos en médula ósea que confirmará el diagnóstico.
En nuestra paciente, se pudieron descartar alteraciones del metabolismo fosfocálcico, dado que no presentaba alteraciones en los valores de calcio y fósforo, y debido a que tampoco presentaba alteraciones fenotípicas, ni hallazgos típicos compatibles con osteogénesis imperfecta11,12, hiperparatiroidismo13, o raquitismo14,15 en las radiografías.
Se puede excluir del diagnóstico diferencial la posibilidad de presentar un Síndrome Mc Cune-Allbright, puesto que no presenta ningún signo de la tríada típica de dicho síndrome (lesiones de displasia fibrosa multifocales, pubertad precoz o pigmentación cutánea en forma de mancha de café con leche)16,17.
Otras etiologías de fracturas patológicas, como tumores óseos malignos y benignos (histiocitosis X, osteoma osteoide, osteoblastoma…), tumores sólidos, osteomielitis aguda o trastorno de la conducta alimentaria con IMC muy bajo, son poco probables en esta paciente.
Comentario final
Ante la presencia de dolor lumbar, se deben descartar las banderas rojas o signos de alarma. Si detectamos signos de alarma, se realizarán pruebas de imagen, siendo de primera elección la radiografía simple. Si encontramos una fractura patológica, debe plantearse el diagnóstico diferencial entre alteraciones del metabolismo fosfocálcico, tumores (óseos o sólidos) y leucemia. Por ello, se solicitará un hemograma y una bioquímica que incluya marcadores del metabolismo fosfocálcico así como una coagulación. Ha de tenerse en cuenta que las fracturas patológicas, aunque muy infrecuentes, pueden ser una forma de presentación de una leucemia.
Bibliografía
- Maher C, Underwood M, Buchbinder
- R. Non-specific low back Lancet 2017; 389:736-747
- Verhagen AP, Downie A, Popal N, Maher C, Koes BW. Red flags presented in current low back pain guidelines: a review. Eur Spine J 2016; 25:2788-802
- García Fontecha C. Dolor de espalda. Pediatr Integral 2014; 18:413-424
- Kordi R, Rostami M. Low Back Pain in children and adolescents: an algorithmic clinical approach. Iran J Pediatr 2011; 21:259-270
- Alonso Hernández J, Egea Gámez R.M. Patología de la espalda. Pediatr Integral 2019; 23:187-193
- Ortiz EJ, Isler MH, Navia JE, Canosa R. Pathologic fractures in children. Clin Orthop Relat Res 2005; 432:116-126
- Lassaletta Atienza A. Leucemia linfoblástica aguda. Pediatr Integral 2016; 20:380-389
- Alos N, Grant RM, Ramsay T, Halton J, Cummings EA, Miettunen PM et al. High incidence of vertebral fractures in children with acute lymphoblastic leukemia 12 months after the initiation of therapy. J Clin Oncol 2012; 30:2760-2767
- Bhojwani D, Yang JJ, Pui CH. Biology of childhood acute lymphoblastic leukemia. Pediatr Clin North Am 2015; 62:47-60
- Sun T. Clinical application. En: Flow Cytometry, Immunochemistry, and Molecular Genetics for Hematologic Neoplasms, 2ª ed. Philadelphia: Lippincott Williams & Wilkins, 2012
- Rauch F, Glorieux FH. Osteogenesis imperfec-
- t Lancet 2004; 363:1377-1385
- Chines A, Petersen DJ, Schranck FW, Whyte MP. Hypercalciuria in children severely affected with osteogenesis imperfecta. J Pediatr 1991; 119:51-57
- De la Calle Cabrera T. Raquitismo carencial. Raquitismos resistentes. Pediatr Integral 2015; 19:477-487
- Silverberg SJ, Bilezikian JP. Evaluation and management of primary hyperparathyroidism. J Clin Endocrinol Metab 1996; 81:2036-2040
- Bilezikian J.P, Brandi M.L, Rubin M, Silverberg SJ. Primary hyperparathyroidism: new concepts in clinical, densitometric and biochemical features. J Intern Med 2005; 257:6-17
- Muñoz Villa A. Rabdomiosarcomas. Pediatr Integral 2016; 20:458-464
- Mejorado Molano FJ, Soriano Guillén L. Pubertad precoz y adelantada. Pediatría Integral 2020; 24:183-190
