Sara López López.
Unidad de Endocrinología Pediátrica. Hospital Universitario Insular Materno Infantil de Canarias (CHUIMI). Las Palmas de Gran Canaria
Introducción
Desde el descubrimiento de la insulina por Banting y Best (1921), el manejo de la diabetes y las herramientas que tenemos a nuestro alcance para conseguir un mejor control metabólico han experimentado cambios inimaginables.
La diabetes tipo 1 (DM1) es una de las enfermedades crónicas más frecuentes en la infancia asociando un riesgo de complicaciones en caso de mal control de la misma. Hay aproximadamente 550.000 niños con DM1 en el mundo y unos 86.000 son diagnosticados anualmente, con una incidencia que no para de incrementar1,2.
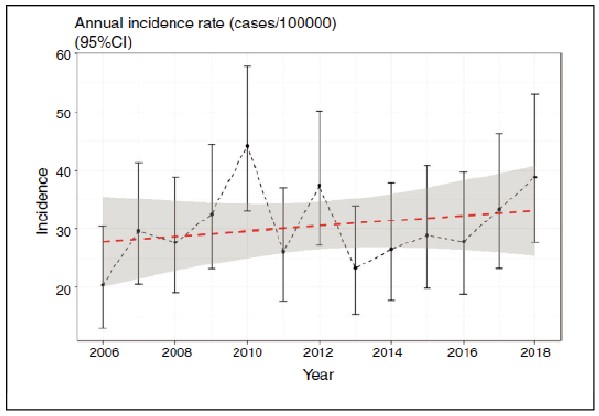
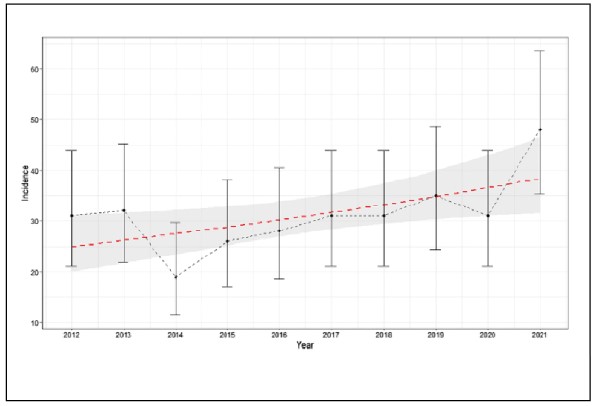
La incidencia media en nuestro país es de aproximadamente 17,7/100.000 habitantes menores de 14 años, con valores que oscilan entre los 7,9/100.000 descritos en Baleares y los 30-36/100.000 en las Islas Canarias3,4. La incidencia global para el período 2006-2018 fue de 30,48/100.000 (IC 95%: 27,74-33,42) en la isla de Gran Canaria (figura 1)4,5. Datos no publicados en la isla de Tenerife (Dr. González Díaz) cifran una incidencia de >30/100.000. En la isla de La Palma la incidencia según datos publicados es de 32/100.000 6 (figura 2).
Según estudios el 40-50% del riesgo genético para desarrollar DM1 está vinculado a un grupo de genes localizados en el cromosoma 6 (6p21). Esta región cromosómica contiene un gran “cluster” o agrupación de genes llamado Complejo Mayor de Histocompatibilidad (MHC o HLA). Las variaciones alélicas en la región HLA de riesgo para la aparición de diabetes son el HLA DRB1*03 y el DRB1*04 así como el DQB1. En concreto, los que presentan un riesgo mayor son: DRB1*0301, DQA1*0501, DQB1*0201, DRB1*0405, DQA1*0301-DQB1*0302, DRB1*0401, DQA1*0301, DQB*0302, DRB1*0402, DQA1*0301, DQB1*0302. Otros con menor riesgo son los haplotipos DRB1*0404, DQA1*0301-DQB1*0302, DRB1*0801, DQB1*0401-DQB1*0402 7.
En Canarias, aproximadamente >70 % de la carga genética es originaria de la península ibérica, 25% del norte de África y un 3% de población subsahariana8. Se ha demostrado la existencia de un enriquecimiento genético de origen africano en genes relacionados con enfermedades prevalentes en Canarias. Uno de esos genes se encuentra en la región correspondiente al HLA en el cromosoma 6. La elevada incidencia de DM1 en países árabes y del norte de África, y la elevada influencia genética de esas regiones en nuestra población hace pensar en un factor genético común que pudiera predisponer a la DM1.
Según datos pendientes de publicar para la Isla de Gran Canaria se han objetivado similitudes entre los HLA estudiados hasta la fecha en cuanto a los alelos DRB1* (DRB1*03 y el DRB1*04) en esta isla comparando con el resto de España con la diferencia de presentar similar prevalencia de DRB1*03 y 04 en Canarias, mientras que hay mayor frecuencia de DRB1*03 en el resto de España. Con respecto a los genes DQB1*, puede que una menor prevalencia de genes protectores (especialmente DQB1*06) que en otras regiones tenga un rol en la mayor incidencia encontrada en nuestra comunidad.
La tasa de incidencia de DM1 en Canarias se sitúa justo después de países como Finlandia, Suecia y la isla de Cerdeña, así como ratios similares a las descritas en Irlanda del Norte (2014-2013), Arabia Saudí y Noruega y mayores que las descritas para el resto de países europeos4. Por lo tanto, las Islas Canarias y algunas regiones del sur de España, así como la isla de Cerdeña, son la excepción al gradiente norte-sur descrito para la incidencia de DM1 en Europa.
Actualidad tecnológica en diabetes
Dispositivos de medias unidades y plumas inteligentes (Smart pens) (tabla I)
Se dispone de dispositivos para administrar medias unidades en función del tipo de insulina:
- Insulinas de acción rápida: Apidra®, Novorapid y Fiasp Penfill®, en cartuchos recargables; Humalog Junior® Kwikpen, en bolígrafo desechable.
- Insulinas de acción prolongada: Lantus® y Tresiba®, en cartuchos recargables.
Existen dos dispositivos:
- JuniorSTAR®: Solo es compatible con cartuchos para plumas recargables de Sanofi (Lantus® insulina glargina 100UI/ml; y Apidra® insulina glulisina)
- NovoPen Echo®: Utiliza cartuchos Penfill® (insulina aspart y fast aspart, Novorapid® y Fiasp®).
Sistemas de monitorización de glucosa (SMG) [sistemas flash (SMFG) y sistemas de monitorización continua de glucosa (SMCG)]9-11
Los SMG son herramientas de tecnología avanzada que realizan una monitorización estrecha de los niveles de glucosa en líquido intersticial de manera continua o intermitente.
Los niveles de glucosa intersticial y capilar no son exactamente lo mismo, ya que la composición del líquido intersticial depende de los intercambios entre las células en el tejido y la sangre.
Cuando el nivel de glucosa en sangre se encuentra estable durante un tiempo, los niveles de la glucosa intersticial y capilar se equilibran y coinciden, pero, cuando hay fluctuaciones de glucosa en sangre, así como hipo o hiperglucemia existe un retardo y/o diferencia de la intersticial respecto a la capilar de unos 5-10 minutos.
Estos sistemas nos permiten conocer al detalle los controles glucémicos que tiene un paciente, la variabilidad de los mismos (CV: coeficiente de variación) así como otras variables importantes para el control metabólico como son: el tiempo en rango (TIR) (tiempo entre 70-180 mg/dl), el tiempo en hipoglucemia (TBR) o hiperglucemia (TAR), glucemia promedio y una estimación de la hemoglobina glicosilada (HbA1c).
Todos los SMG tienen un sensor o electrodo (pequeño filamento que se coloca a nivel subcutáneo con un aplicador) y que, mediante una reacción enzimática, va midiendo los valores de glucosa intersticial proporcionando lecturas en pocos minutos. Este sensor enviará los datos al resto de componentes de los distintos SMG.
Para evaluar la exactitud y la fiabilidad de cada SMG, en relación a otros parámetros o estándares considerados de referencia (glucosa basal, capilar…), existen distintos procedimientos, entre los más aceptados el Mean Absolute Relative Difference (MARD) que expresa la diferencia media entre la medición del sistema y el estándar de referencia de valores de glucemia capilar.
Estos SMG aportan distinta información en relación a los niveles de glucosa permitiendo optimizar el tratamiento, y mejorar en muchos pacientes la calidad de vida. Concretamente aportan:
- Datos numéricos de glucosa intersticial
- Flechas de tendencia que avisan de la dirección (flecha hacia arriba o hacia abajo) y velocidad (nº de flechas) de aumento o descenso de la glucosa intersticial
- Gráficos de glucemias
- Alarmas
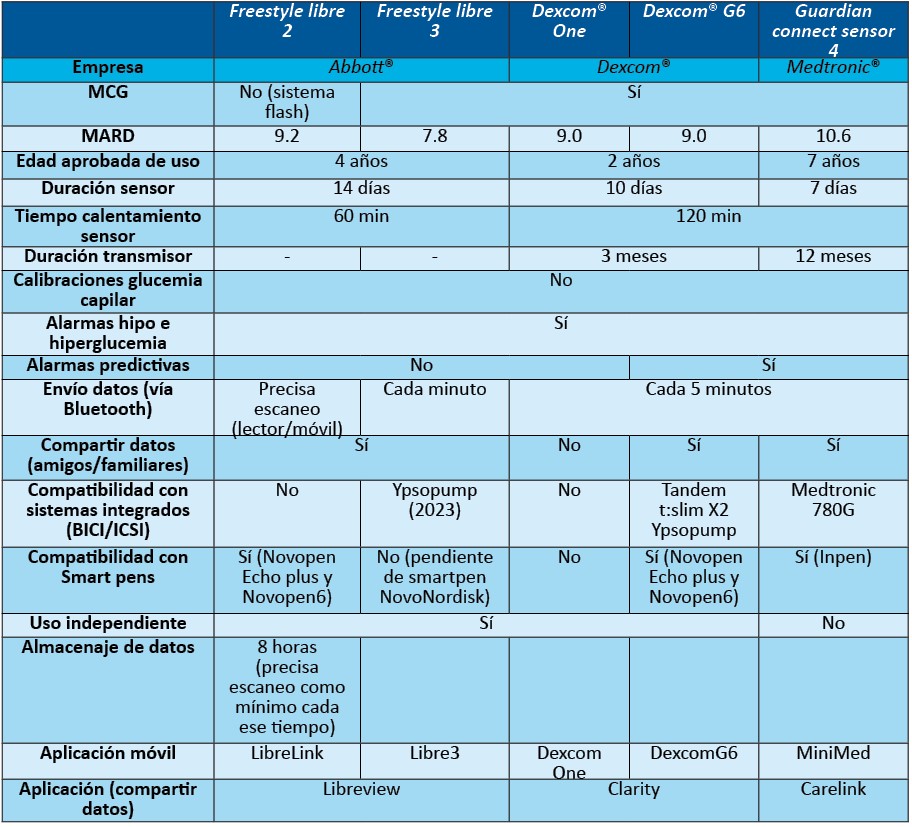
Existen dos tipos de SMG: los sistemas de monitorización de glucosa tipo flash (SMFG) y los sistemas de monitorización continua de glucosa (SMCG) (en tiempo real).
Sistemas de monitorización de glucosa flash (SMFG).
Actualmente solo existe en el mercado el Freestyle Libre2 (Abbott®). Un sensor o pequeño filamento que se inserta con un aplicador en el tejido subcutáneo, y va midiendo cada minuto los valores de glucosa intersticial. Se mantiene en contacto con la piel mediante un adhesivo. Almacena los datos hasta 8 horas (tabla II).
Un lector/móvil (receptor), dispositivo que escanea el sensor y puede visualizar los resultados obteniendo así datos, como los niveles, tendencia de la glucosa y las gráficas. Para obtener una visión global de la glucosa debe realizarse al menos un escaneo cada 8 horas. Dispone de aplicaciones para descargar en el móvil.
No muestra alertas a tiempo real de las hipo o hiperglucemias, si bien los últimos modelos incorporan alarmas personalizadas opcionales para detectar hipoglucemias e hiperglucemias y alarma de pérdida de señal.
Sistemas de monitorización continua de glucosa (SMCG).
Almacenan datos y los transmiten al receptor en tiempo real, pudiendo integrarse con bombas de infusión continua de insulina (tabla II).
Entre sus componentes básicos están:
- Un sensor que se introduce en el tejido subcutáneo con un aplicador
- Un transmisor (acoplado al sensor) que recopila las lecturas de este y las envía por bluetooth al receptor (bomba de insulina, monitor, móvil…) mediante aplicaciones informáticas que permiten compartirlos con otros usuarios y profesionales sanitarios (algunos en tiempo real y otros mediante descargas por parte del paciente).
En función de los datos detectados de glucemia, pueden predecir hipoglucemias y evitarlas, incluso llegar a suspender la infusión de insulina si están conectados a una bomba. También reducen eventos de hiperglucemia. Para ello disponen de alarmas programables ante hipo o hiperglucemias, o cuando los niveles de glucosa se desvían de un valor preestablecido para poder adoptar medidas.
Dexcom® G7 12. Aprobado en EEUU >2 años. Pendiente de comercialización en España (ya tiene marcado de conformidad europea, CE). Es la última versión tras el G6, siendo de menor tamaño, solo 30 minutos de calentamiento, 12 horas extras de duración, mayor precisión (MARD de 8.2) y con sistema transmisor + sensor integrado.
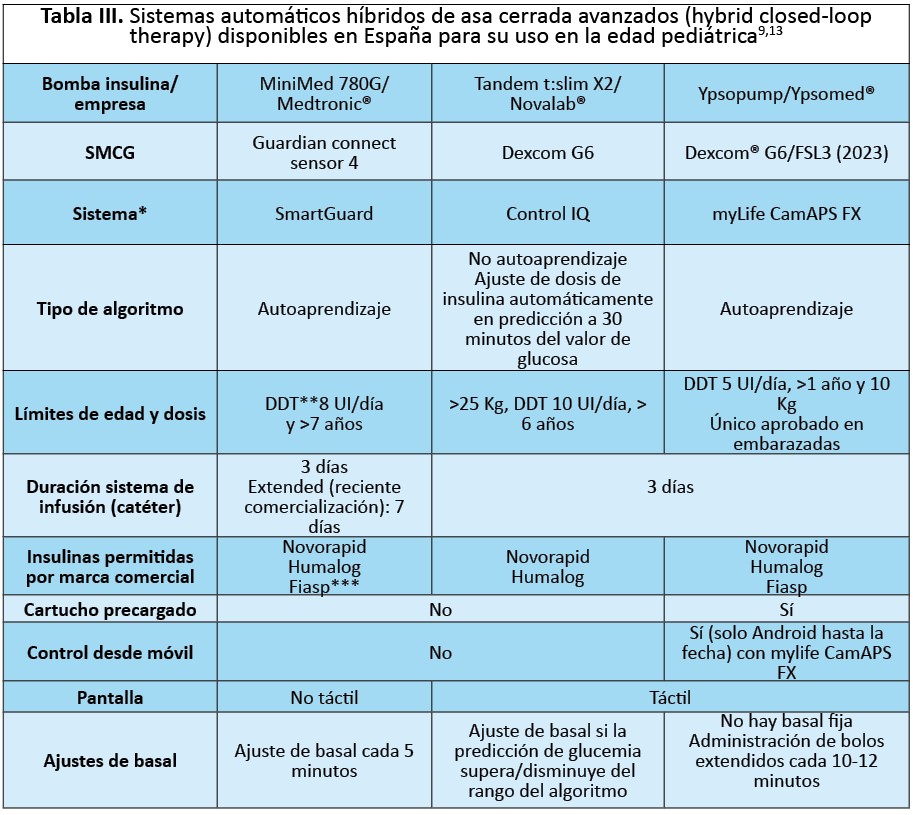
Sistemas automáticos híbridos de asa cerrada avanzados. SMCG-terapia con infusión subcutánea continua de insulina (ICSI-BICI)13,14 (Tabla III)
El mayor reto en el tratamiento de la DM1 es simular el funcionamiento del páncreas.
La terapia con bomba de insulina lleva disponible más de 40 años y en este tiempo se ha perfeccionado hasta conseguir los sistemas comercializados actualmente, en su mayoría híbridos automáticos avanzados de asa cerrada.
Son dispositivos que administran insulina subcutánea de forma continua. Utiliza análogos de acción rápida o ultrarápida. Administran la insulina de manera dual: bolo y basal o en bolos extendidos. La dosis de insulina basal se programa de forma horaria.
Los objetivos son la administración más fisiológica de la insulina, minimizar la variabilidad glucémica y las hipoglucemias. Según el modelo y su algoritmo de control, así como la automatización son capaces de modificar la tasa basal e infundir bolos correctores automáticos.
Son híbridos y no podemos definirlos como páncreas artificial automatizado porque el bolo previo a las comidas todavía precisa de nuestra intervención activa y no es automático.
El paciente precisa para su funcionamiento adecuado de un:
- SMCG (adecuado a cada sistema) o sensor de glucosa
- Sistema de infusión continua de insulina o bomba de insulina
- Equipo de infusión (cánula de inserción en piel y tubo de conexión paciente-bomba de insulina)
- Reservorio de insulina/cartucho de insulina precargado/a rellenar
- Un algoritmo matemático de control (propio de cada sistema)
Recomendaciones de inicio de la terapia de infusión continua de insulina (ICSI-BICI) en la edad pediátrica
Desde el año 2007, “the Consensus statement from the European Society for Paediatric Endocrinology, the Lawson Wilkins Pediatric Endocrine Society and the International Society for Pediatric and Adolescent Diabetes, endorsed by the American Diabetes Association and the European Association for the Study of Diabetes”15 recomienda el uso de sistemas de infusión continua de insulina en todo niño con DM1 siempre que no haya ninguna contraindicación.
En 2010 se redactó un documento – consenso sobre el tratamiento con infusión subcutánea continua de insulina en DM1 en la edad pediátrica16 que respalda lo previamente comentado: “de acuerdo con los consensos internacionales todos los pacientes pediátricos con DM1 son candidatos potenciales para el uso de ICSI-BICI sin ningún límite de edad ni momento evolutivo de la enfermedad”. También la Sociedad Española de Diabetes (SED) avala esto último17.
En menores de 7 años, según últimas recomendaciones de la ISPAD 2022 (International Society for Pediatric and Adolescent Diabetes)18 en el manejo del niño menor de esta edad figuran estos sistemas ICSI-BICI como el modo de infusión de insulina de primera elección.
Por tanto, las BICI-ICSI están recomendadas para todos los pacientes pediátricos con DM1.
Contraindicaciones para el uso de terapia de infusión continua de insulina (ICSI-BICI)
- Preferencia de la persona con diabetes a no usar tecnología.
- Alergia, irritación de la piel por sensor/BICI o dificultades para llevar incorporado un SMCG
*Tanto el sistema integrado Medtronic 780G como el de Tandem t:slimX2 pueden utilizarse en modo manual (en parada predictiva de hipoglucemia) en aquellos pacientes que no puedan utilizar por edad o dosis de insulina diaria total
**DDT (dosis diaria total de insulina)
***Diferentes estudios apoyan su uso, aún no recogida en Guía de Uso del sistema MiniMed™ 780G 19,20,21
Otros dispositivos de infusión subcutánea de insulina
I-port Advance® (Medtronic)22,23
- Longitud: cánula suave disponible en largos de 6 mm y 9 mm.
- Compatibilidad: las agujas utilizadas con el puerto de inyección deben tener entre 5 y 8 mm de largo.
- Tiempo de uso: Hasta 72 horas, o hasta 75 inyecciones, lo que ocurra primero.
Otras novedades
Baqsimi® 3 mg (glucagón intranasal)24,25
Tiene por ficha técnica un uso permitido en > 4 años. Fue aprobado por la Unión Europea e iniciada la comercialización en España en enero 2021. No requiere inhalación ni reconstituirse, ya viene preparado para absorción pasiva por mucosa nasal. No necesita refrigeración, a temperatura ambiente hasta 30ºC. Es muy sencillo de administrar.
Es una medicación que precisa visado. Actualmente en Canarias solo está disponible para pacientes menores de 18 años en tratamiento con insulina con alto riesgo de hipoglucemias graves con pérdida de consciencia. Presenta escasos efectos secundarios: lagrimeo, irritación del tracto respiratorio superior, náuseas, cefalea, vómitos.
¿Hacia dónde vamos?
Bombas de parche (“patch”) 9,26-31
La mayoría de las bombas de insulina requieren un catéter desde la bomba hasta el sitio de infusión, pero existe una alternativa (patch). En ella la insulina se administra directamente desde una cápsula adherida a la piel, con un equipo de infusión integrado o muy corto.
- Omnipod® 5 (Insulet). Aprobada por la Food and Drug Administration en enero de 2022. Tiene marcado de conformidad europea (CE) desde septiembre 2022 pero no disponible en España. Es el primer sistema de asa cerrada que se puede controlar completamente desde una aplicación en el móvil con tecnología SmartAdjust (integrada con el SMCG Dexcom G6).
- Glucomen® Day Pump (Menarini). Inicio de comercialización en 2023 en España. Ausencia de integración con SMCG actualmente.
- Accu-chek® Solo (Roche)
- TouchCare® sistema Nano (Medtrum)
Do-it-yourself (DIY)9,32
Hace unos años surgió el movimiento #WeAreNotWaiting defendiendo que la tecnología avanzaba con mayor rapidez que los dispositivos para la diabetes.
Los sistemas denominados “do-it-yourself” para la administración automatizada de insulina usan los SMCG y las bombas de insulina existentes que se vinculan mediante un algoritmo de código abierto. El proyecto Open Artificial Pancreas System (OpenAPS) es gratuito, de código abierto, para que la tecnología básica del páncreas artificial esté disponible para todos. No obstante, estos dispositivos no han pasado por el escrutinio de la aprobación regulatoria por lo que los usuarios deben ser conscientes de que no existe un marco regulatorio actual para ello.
Páncreas bihormonal de insulina y glucagón9,33
Otros sistemas que están en desarrollo son los denominados bihormonales para la administración automatizada de insulina en los que se emplea glucagón e insulina a través de un sistema totalmente automático. Son sistemas hasta la fecha más complejos, con un coste más elevado y con mayor número de efectos secundarios debidos al glucagón (náuseas, vómitos y cefalea), así como un aumento de la hiperglucemia por el uso inadecuado del glucagón y la inestabilidad de las formulaciones.
Por otro lado, los SMCG se hacen más pequeños y precisos para intentar proporcionar mejores herramientas que permitan un óptimo control metabólico y calidad de vida en las personas con DM1.
Conclusiones
Gracias a la tecnología el control metabólico de la diabetes ha sufrido una revolución en estos últimos años, ya que nos aportan más información del día a día de los pacientes con DM1, así como mejoría en la calidad de vida34-38.
No podemos olvidar que se han realizado avances en la terapia con células madre, siendo la vía de investigación más avanzada para una cura definitiva de la diabetes9,39.
Pero en la actualidad, la tecnología en diabetes es el camino en el manejo de esta enfermedad permitiendo a los pacientes y a sus familias una mayor libertad de elección y responsabilidad en la toma de decisiones.
Bibliografía
- Frontino G, Guercio Nuzio S, Scaramuzza A, D’Annunzio G, Toni S, Citriniti F et al. Prevention of type 1 diabetes: where we are and where we are going. Minerva Pediatr (Torino) 2021; 73:486-503. https://doi.org/10.23736/S2724-5276.21.06529-0
- Ogle GD, James S, Dabelea D, Pihoker C, Svennson J, Maniam J et al. Global estimates of incidence of type 1 diabetes in children and adolescents: Results from the International Diabetes Federation Atlas, 10th edition. Diabetes Res Clin Pract 2022; 183:109083. https://doi.org/10.1016/j.diabres.2021.109083
- Nóvoa Medina Y. Change over time in the incidence of type 1 diabetes mellitus in Spanish children. Endocrinol Diabetes Nutr (Engl Ed) 2018; 65:65-67. https://doi.org/10.1016/j.endinu.2017.11.010
- Nóvoa Y, de La Cuesta A, Caballero E, de Gauna MR, Quinteiro S, Domínguez A et al. Epidemiology of childhood-onset type 1 diabetes in Gran Canaria (2006-2018). Endocrinol Diabetes Nutr (Engl Ed) 2020; 67:658-664. https://doi.org/10.1016/j.endinu.2019.11.010
- Nóvoa-Medina Y, Pavlovic-Nesic S, González-Martín JM, Hernández-Betancor A, López S, Domínguez-García A et al. Role of the SARS-CoV-2 virus in the appearance of new onset type 1 diabetes mellitus in children in Gran Canaria, Spain. J Pediatr Endocrinol Metab 2022; 35:393-397. https://doi.org/10.1515/jpem-2021-0727
- Belinchón BM, Hernández Bayo JA, Cabrera Rodríguez R. Incidence of childhood type 1 diabetes (0-14yrs) in La Palma Island. Diabetologia 2008; 51(Suppl 1):S5-564
- Erlich H, Valdes AM, Noble J, Carlson JA, Varney M, Concannon P et al, Type 1 Diabetes Genetics Consortium. HLA DR-DQ haplotypes and genotypes and type 1 diabetes risk: analysis of the type 1 diabetes genetics consortium families. Diabetes 2008; 57:1084-1092. https://doi.org/10.2337/db07-1331
- Guillen-Guio B, Lorenzo-Salazar JM, González-Montelongo R, Díaz-de Usera A, Marcelino-Rodríguez I, Corrales A et al. Genomic Analyses of Human European Diversity at the Southwestern Edge: Isolation, African Influence and Disease Associations in the Canary Islands. Mol Biol Evol 2018; 35:3010-3026. https://doi.org/10.1093/molbev/msy190
- Guijo Alonso B, Alkadi Fernández K, Yelmo Valverde R, Pérez Repiso V, García Cuartero B. Nuevas tecnologías y nuevos retos en la diabetes en la edad pediátrica Rev Esp Endocrinol Pediatr 2022; 13:34-45. https://www.endocrinologiapediatrica.org/revistas/P1-E41/P1-E41-S3839-A766.pdf
- Grupo de Trabajo de Tecnologías Aplicadas a la Diabetes. Sociedad Española de Diabetes (SED). Monitorización continua de glucosa y monitorización flash de glu-cosa 2018
- Solá Izquierdo E. Actualización en los sistemas de monitorización continua de glu-cosa en diabetes. Nov 21, 2022. https://www.revistadiabetes.org/wp-content/uploads/Actualizacion-en-los-sistemas-de-monitorizacion-continua-de-glucosa-en-diabetes.pdf
- https://www.dexcom.com/en-us/g7-cgm-system
- Grupo de Trabajo de Tecnologías Aplicadas a la Diabetes. Sociedad Española de Diabetes (SED). Sistemas de asa cerrada 2021
- Griffin TP, Gallen G, Hartnell S, Crabtree T, Holloway M, Gibb FW et al. UK’s Association of British Clinical Diabetologist’s Diabetes Technology Network (ABCD-DTN): Best practice guide for hybrid closed-loop therapy. Diabet Med. 2023 Mar 18:e15078. https://doi.org/10.1111/dme.15078
- Phillip M, Battelino T, Rodriguez H, Danne T, Kaufman F; European Society for Paediatric Endocrinology; Lawson Wilkins Pediatric Endocrine Society; International Society for Pediatric and Adolescent Diabetes; American Diabetes Association; European Association for the Study of Diabetes. Use of insulin pump therapy in the pediatric age-group: consensus statement from the European Society for Paediatric Endocrinology, the Lawson Wilkins Pediatric Endocrine Society, and the International Society for Pediatric and Adolescent Diabetes, endorsed by the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 2007; 30:1653-1662. doi:10.2337/dc07-9922
- Barrio Castellanos R, García Cuartero B, Gómez Gila A, González Casado I, Hermoso López F, Luzuriaga Tomás C et al.; Grupo de Trabajo de Diabetes Pediátrica de la Sociedad Española de Endocrinología Pediátrica (SEEP). Documento de consenso sobre tratamiento con infusión subcutánea continua de insulina de la diabetes tipo 1 en la edad pediátrica An Pediatr (Barc) 2010; 72:352.e1-4. doi: 10.1016/j.anpedi.2010.01.009
- Barrio Castellanos R, Martín Vaquero P. Capítulo 1. ISCI: Infusión subcutánea continua de insulina. https://www.sediabetes.org/wp-content/uploads/tecnologias-aplicadas.pdf
- Sherr JL, Schoelwer M, Dos Santos TJ, Reddy L, Biester T, Galderisi A et al. ISPAD Clinical Practice Consensus Guidelines 2022: Diabetes technologies: Insulin delivery. Pediatr Diabetes 2022; 23:1406-1431. doi:10.1111/pedi.13421
- González de Buitrago Amigo J, González García A, Díaz Fernández P, Fernández Llamas M, Tejado Bravo ML, de Nicolás Jiménez JM, Ferrer Lozano M. The impact of “faster aspart” on blood glucose control in children and adolescents with type 1 diabetes treated using a sensor-augmented insulin pump. An Pediatr (Engl Ed) 2021; 95:321-329. https://doi.org/10.1016/j.anpedi.2020.11.002
- Hsu L, Buckingham B, Basina M, Ekhlaspour L, von Eyben R, Wang J et al. Fast-Acting insulin aspart use with the MiniMedTM 670G System. Diabetes Technol Ther 2021; 23:1-7. https://doi.org/10.1089/dia.2020.0083
- Lee MH, Paldus B, Vogrin S, Morrison D, Zaharieva DP, Lu J et al. Fast-Acting insulin aspart versus insulin aspart using a second-generation hybrid closed-loop system in adults with type 1 diabetes: A randomized, open-label, crossover trial. Diabetes Care 2021 Aug 6:dc210814. https://doi.org/10.2337/dc21-0814
- https://www.medtronic-diabetes.com/es-ES/accesorios/i-port-advance-puerto-de-inyeccion
- http://www.medihc.com.mx/iport
- https://www.ema.europa.eu/en/documents/product-information/baqsimi-epar-product-information_es.pdf
- https://www.youtube.com/watch?v=uTWKxAovnuc
- Cobry EC, Berget C, Messer LH, Forlenza GP. Review of the Omnipod® 5 Automated Glucose Control System Powered by Horizon™ for the treatment ofType 1 diabetes. Ther Deliv 2020; 11:507-519. https://doi.org/10.4155/tde-2020-0055
- Ly TT, Layne JE, Huyett LM, Nazzaro D, O’Connor JB. Novel Bluetooth-Enabled Tubeless Insulin Pump: Innovating Pump Therapy for Patients in the Digital Age. J Diabetes Sci Technol 2019; 13:20-26. https://doi.org/10.1177/1932296818798836
- Danne T, Schwandt A, Biester T, Heidtmann B, Rami-Merhar B, Haberland H et al.; DPV Initiative. Long-term study of tubeless insulin pump therapy compared to multiple daily injections in youth with type 1 diabetes: Data from the German/Austrian DPV registry. Pediatr Diabetes 2018; 19:979-984. https://doi.org/10.1111/pedi.12658
- Layne JE, Huyett LM, Ly TT. Glycemic Control and Factors Impacting Treatment Choice in Tubeless Insulin Pump Users: A Survey of the T1D Exchange Glu Online Community. J Diabetes Sci Technol 2019; 13:1180-1181. https://doi.org/10.1177/1932296819868698
- Kulzer B, Freckmann G, Heinemann L, Schnell O, Hinzmann R, Ziegler R. Patch Pumps: What are the advantages for people with diabetes? Diabetes Res Clin Pract 2022; 187:109858. https://doi.org/10.1016/j.diabres.2022.109858
- Ziegler R, Oliver N, Waldenmaier D, Mende J, Haug C, Freckmann G. Evaluation of the accuracy of current tubeless pumps for continuous subcutaneous insulin infusion. Diabetes Technol Ther 2021; 23:350-357. https://doi.org/10.1089/dia.2020.0525
- Morrison AE, Chong K, Senior PA, Lam A. A scoping review of Do-It-Yourself Automated Insulin Delivery system (DIY AID) use in people with type 1 diabetes. PLoS One 2022; 17:e0271096. https://doi.org/10.1371/journal.pone.0271096
- Herrero P. ¿Qué aportan y qué indicaciones tendrán los sistemas de páncreas artifi-cial bihormonales de insulina y glucagón? Diabetes 2021; 69: 24-27. https://www.revistadiabetes.org/investigacion/que-aportan-y-que-indicaciones-tendran-los-sistemas-de-pancreas-artificial-bihormonales-de-insulina-y-glucagon/
- Haynes E, Ley M, Talbot P, Dunbar M, Cummings E. Insulin pump therapy improves quality of life of young patients with type 1 diabetes enrolled in a government-funded insulin pump program: A qualitative study. Can J Diabetes 2021; 45:395-402. https://doi.org/10.1016/j.jcjd.2020.08.101
- Burckhardt MA, Smith GJ, Cooper MN, Jones TW, Davis EA. Real-world outcomes of insulin pump compared to injection therapy in a population-based sample of children with type 1 diabetes. Pediatr Diabetes 2018; 19:1459-1466. https://doi.org/10.1111/pedi.12754
- Mueller-Godeffroy E, Vonthein R, Ludwig-Seibold C, Heidtmann B, Boettcher C, Kramer M et al.; German Working Group for Pediatric Pump Therapy (agip). Psychosocial benefits of insulin pump therapy in children with diabetes type 1 and their families: The pumpkin multicenter randomized controlled trial. Pediatr Diabetes 2018; 19:1471-1480. https://doi.org/10.1111/pedi.12777
- Fureman AL, Lilja M, Lind T, Särnblad S, Bladh M, Samuelsson U. Comparing continuous subcutaneous insulin infusion and multiple daily injections in children with Type 1 diabetes in Sweden from 2011 to 2016-A longitudinal study from the Swedish National Quality Register (SWEDIABKIDS). Pediatr Diabetes 2021; 22:766-775. https://doi.org/10.1111/pedi.13217
- Auzanneau M, Karges B, Neu A, Kapellen T, Wudy SA, Grasemann C, Krauch G, Gerstl EM, Däublin G, Holl RW. Use of insulin pump therapy is associated with reduced hospital-days in the long-term: a real-world study of 48,756 pediatric patients with type 1 diabetes. Eur J Pediatr 2021; 180:597-606. https://doi.org/10.1007/s00431-020-03883-2
- Inoue R, Nishiyama K, Li J, Miyashita D, Ono M, Terauchi Y et al. The feasibility and applicability of stem cell therapy for the cure of type 1 diabetes. Cells 2021; 10:1589. https://doi.org/10.3390/cells10071589

![Tabla I. Plumas inteligentes (Smart pens)9 [capaces de conectarse con los sistemas de monitorización de glucosa (SMG)]](https://scptfe.com/wp-content/uploads/2023/07/47-2-tabla-I-Avances-tecnologicos.jpg)